バイオマテリアル(医用材料)
バイオマテリアルとティッシュエンジニアリング
1.ティッシュエンジニアリングとは
人工臓器は、従来の汎用高分子や金属、セラミクスなどの材料を成形・加工して用いる方向から、細胞やその集合体である組織、器官、臓器の機能が明らかになるにつれ、細胞が本来有する生物的な機能を利用したバイオハイブリッド型人工臓器の開発へと発展している。さらに最近では、遺伝子工学、分子生物学、細胞工学などの台頭と医療分野への応用を考える中で、組織工学?ティッシュエンジニアリング?の重要性が認識され、その開発が急務となっている。英語でいうTissue Engineeringは国内では研究者によってさまざまな認識があり、研究のアプローチの仕方から、カタカナで単に「ティッシュエンジニアリング」という場合と、「組織工学」、「再生医療」、「再生医工学」、あるいは幹細胞(ES細胞など)を用いて組織の発生から制御し、構築しようという「発生工学」という日本語訳を用いて表現されている。いずれも、in vitro、あるいはin vivoで組織様構造を形成、再構築し、生体内で高機能の組織を再構成させることを主眼においている。この成功は、患者のQOLの向上につながる。Tissue engineeringを最初に提唱したVancantiによれば、「生体機能の回復、維持、改善を可能とする臓器、あるいは代用器官を工学、生命科学の協力の下で開発することを目的とする」研究分野である。生体組織は、肝臓や腎臓などにみられるように、複数種の細胞が作り上げる器官特異的な構造を有し、各器官に特長的な機能を発現している。病気などでその機能が失われたときに、新しく、あるいは補完として生体内、生体外で組織構造を再生・再構築する技術が組織工学の目指すところである。
2.バイオマテリアルとティッシュエンジニアリング
生体組織は細胞だけから構成されているわけではなく、細胞が接着する足場としての細胞外マトリックス、さらに細胞の機能を発現するときに必須となる種々の生理活性物質からの刺激が組織を構成する。すなわち、最近注目されているES細胞などの幹細胞さえ自由に目的の細胞に分化できれば組織の補完・再生が成功するわけではなく、上記の3つが相補的に関わって適時に適当な刺激を受けることで組織が再生できることになる。この点からも細胞の足場、あるいは刺激物質としてのバイオマテリアルの研究なくしては組織工学は成立しない。
3.生分解性マトリクスを用いたティッシュエンジニアリング
これまでに、人工材料上に生体細胞を培養してハイブリッド型人工臓器として生体に埋入することで部分的に生体機能を利用する研究が行われてきている。これは、組織工学の一部をなす研究である。この場合、細胞が接着する足場はその大きさが固定されており、かつ、材料の生体適合性が長期の利用に不可欠である。現状では、いったん埋入・移植した人工材料が一生、生体内で保持されることはほとんどない。また、大きさが変化しないことから小児に移植した場合は、成長にあわせて新しいものに換える手術が避けられない。そこで、生体由来、あるいは合成の生分解性高分子からなる足場を利用して細胞組織を構築すると、生体に生着する可能性があるばかりでなく、成長にともなって足場は分解される一方、組織は発達するので本来の組織と損分なく機能することが期待できる。実際、多孔性のポリ乳酸(写真1)で調製された基材に軟骨細胞を播種・培養することで、種々の軟骨組織が作成できる。人間の耳の形の組織がネズミの背中に生えている写真を見たことがある方もいるだろう。これは、ポリ乳酸の多孔性マトリクスを耳介型に作製し、ここに軟骨細胞を増殖させて作製したもので、組織工学の応用を例示している。このような細胞の足場には、ポリ乳酸ばかりでなく、ポリグリコール酸、ポリ?-カプロラクトン、などの生分解性ポリエステル類、コラーゲンやその熱変性体のゼラチン、多糖類のヒアルロン酸、蟹などの甲羅の成分であるキチン、藻類から採取されるアルギン酸など多岐にわたるマトリクスが利用されている。たとえば、多孔性のポリ乳酸に血管を形成する細胞を移植すると、細胞が再配列して生体中の血管構造と同等の構造を形成し、組織工学的に血管を調製できる。マトリクスのポリ乳酸は生体内で徐々に分解されつつ、生体のもつ再生能力で適当な足場に置き換わっていくために将来的に生体血管と見まがうことのない加齢とともに成長する血管が形成される。熱傷患者の皮膚移植のために切手大の患者の皮膚をコラーゲンからなる人工マトリクス上で培養し、はがき大の大きさにして移植する、という方法も形成外科領域では行われている。培養神経管、培養気管などもこのような手法によって再生されつつある。

4.「細胞シート工学」からのティッシュエンジニアリングのアプローチ
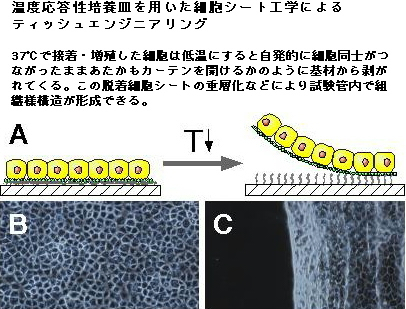
生体組織の構造を見直すと、種々の細胞がシートを形成し、これが層構造をなして組織が構成されていることがわかる。そこで、種々の細胞を培養して細胞シートを構築し、これらのシートを重ね合わせることで組織様構造を形成する、「細胞シート工学」による組織構築の検討が推進されている。通常の細胞培養では、培養した細胞を培養基材から脱着・回収するのにトリプシンなどのタンパク質分解酵素とEDTAなどのキレート剤を併用して行われる。このとき細胞膜表面で機能を発現している膜タンパクも同時に傷害されるために、細胞組織が構築されたときに発現される機能がほとんどみられない、あるいは低下することがまま生起する。そこで、増殖した培養細胞を単層の組織として回収する手法が検討されている。このとき、酵素処理をすることなく細胞を脱着できる表面が必要となる。この目的のために、温度変化に応答して水中で溶解・不溶化変化を示すポリ(N-イソプロピルアクリルアミド)(PIPAAm)を化学的に結合させた表面が考えられた。この表面は37°Cの培養温度で細胞が接着・増殖する一方、温度を32℃以下にすると増殖した細胞は単層シートのまま脱着・回収できる(写真2)。このとき、脱着細胞の下面には培養液から、あるいは細胞自身が産生した細胞外マトリクス成分が存在し、これがあたかも「糊」のごとく作用するために、新しい基材にシートのまま再接着させることが可能である。この手法を用いれば、同種、異種機能を有する細胞シートに重層化させて細胞組織用構造を試験管内で形成でき、この組織は互いに協調して高い生理機能を発現することが明らかとなりつつある。東京女子医科大学と大阪大学との共同研究から心筋梗塞モデルの動物の心臓に、この手法で作製した重層化心筋細胞シートをあたかもセロハンテープを貼るかのごとく移植すると、心筋シートの持つ収縮性の結果、心機能が回復していることが確認された。また、皮膚移植にも応用可能で、倫理委員会の承認のもと、熱傷患者への表皮細胞シート移植が行われ、良好な回復を示していることが明らかとなりつつある。この手法は世界に先駆けて達成された手法であり、日本発の組織工学とそれを利用した治療システムが構築できることを示した好例である。
このように、組織工学を利用した治療システムの構築は、今後ますます人工臓器分野や臨床分野で重要な位置を占めることになると考えられる。この成功と発展のためには、さらに遺伝子工学、分子生物学、細胞工学、材料工学、そして医学との密接な連携が重要であることは疑うまでもない。(菊池明彦)
このページの内容には万全を期しておりますがその内容を保証するものではありません。
このぺージは情報提供を目的としておりますが最終判断は自己責任でお願いします。
このページの内容によって生じたいかなる損害も日本人工臓器学会では負いかねます。